Ejercicio Resuelto sobre Calorimetría
publicidad
Una licuadora, cuyo motor tiene una potencia de 90 W, se utiliza para agitar 200 g de agua durante 1 minuto. La licuadora pierde el 10% de su energía por disipación, mientras que el otro 90% de la energía corresponde al trabajo del motor transferido en forma de calor al agua dentro de la licuadora. Calcule el aumento de temperatura de la masa de agua. Dado: 1 cal = 4,2 J.
Datos del problema:
- Potencia de la licuadora: \( \mathscr P = 90 W \);
- Energía perdida por disipación: Ed = 10% E;
- Masa de agua: m = 200 g;
- Intervalo de tiempo: Δt = 1 min;
- Calor específico del agua: c = 1 cal/g°C;
- Equivalente mecánico del calor: 1 cal = 4,2 J.
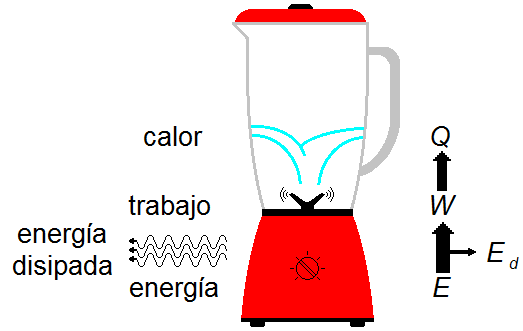
De la energía total E producida por el motor, el 10% se pierde por disipación Ed
(en forma de calor y sonido producido por la licuadora), mientras que el otro 90% de la energía se
utiliza en el trabajo W para producir calor Q, que calienta el agua (Figura 1).
\[
\begin{gather}
E-E_d=W=Q
\end{gather}
\]
Solución:
Convirtiendo el intervalo de tiempo dado en minutos (min) a segundos (s)
\[
\begin{gather}
\Delta t=1\;\mathrm{\cancel{min}}\times\frac{60\;\mathrm s}{1\;\mathrm{\cancel{min}}}=60\;\mathrm s
\end{gather}
\]
La energía producida por la licuadora durante el tiempo de funcionamiento se calcula con
\[
\begin{gather}
\bbox[#99CCFF,10px]
{\mathscr P=\frac{E}{\Delta t}}
\end{gather}
\]
\[
\begin{gather}
E=\mathscr P\Delta t \\[5pt]
E=90\times 60 \\[5pt]
E=5400\;\mathrm J
\end{gather}
\]
La energía disipada será
\[
\begin{gather}
E_d=10\text{%}E \\[5pt]
E_d=\frac{10}{100}\times 5400 \\[5pt]
E_d=0,1\times 5400 \\[5pt]
E_d=540\;\mathrm J
\end{gather}
\]
La energía utilizada en el trabajo para calentar el agua será
\[
\begin{gather}
W=E-E_d \\[5pt]
W=5400-540 \\[5pt]
W=4860\;\mathrm J
\end{gather}
\]
Convirtiendo la energía calculada en julios (J) a calorías (cal) según el problema
\[
\begin{gather}
W=4860\;\mathrm{\cancel J}\times\frac{1\;\mathrm{cal}}{4,2\;\mathrm{\cancel J}}\approx 1157\;\mathrm{cal}
\end{gather}
\]
\[
\begin{gather}
W=Q\approx 1157\;\mathrm{cal}
\end{gather}
\]
La ecuación del calor está dada por
\[
\begin{gather}
\bbox[#99CCFF,10px]
{Q=mc\Delta\theta}
\end{gather}
\]
\[
\begin{gather}
\Delta\theta=\frac{Q}{mc} \\[5pt]
\Delta\theta=\frac{1157}{200\times 1}
\end{gather}
\]
\[
\begin{gather}
\bbox[#FFCCCC,10px]
{\Delta\theta\approx 5,8\;\mathrm{°C}}
\end{gather}
\]
Observación: para la temperatura se utilizó el símbolo θ para no confundir con
t usado para el intervalo de tiempo en la fórmula de la potencia.
publicidad

Fisicaexe - Physics Solved Problems by Elcio Brandani Mondadori is licensed under a Creative Commons Attribution-NonCommercial-ShareAlike 4.0 International License .