Exercício Resolvido de Termodinâmica
publicidade
Um gás perfeito tem um volume inicial de 3,0 litros. Expande-se isotermicamente a 300 kelvins até que seu volume dobre. Se a expansão tivesse ocorrido a 600 kelvins, qual a relação entre os trabalhos realizados pelo gás?
Dados do problema:
- Volume inicial: V1 = 3,0 ℓ;
- Volume final: V2 = 6,0 ℓ;
- Temperatura da primeira expansão: T1 = 300 K;
- Temperatura da segunda expansão: T2 = 600 K.
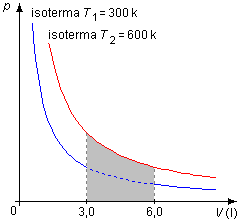
O gráfico de uma transformação isotérmica é uma hipérbole, com a curva da temperatura mais alta em uma
posição mais afastada dos eixos P e V.
Solução
O trabalho \( \large{\tau} \) será calculado pela área sob a curva do Gráfico 1 entre os volumes, inicial (V1) e final V2, para uma transformação isotérmica está área é calculada pela seguinte fórmula
\[ \bbox[#99CCFF,10px]
{\large{\tau} =nRT\ln \left(\,\frac{V_{2}}{V_{1}}\,\right)}
\]
Para a transformação à temperatura de 300 K o trabalho será, pelo Gráfico 2
\[
\begin{gather}
{\large{\tau}}_{1}=nRT\ln\left(\frac{V_{2}}{V_{1}}\right)\\
{\large{\tau}}_{1}=300nR\ln\left(\frac{6,0}{3,0}\right) \tag{I}
\end{gather}
\]
representado pela área em cinza sob a isoterma de T1=300 K (em azul no gráfico).
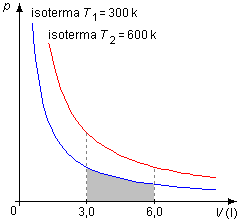
Para a transformação à temperatura de 600 K o trabalho será, pelo Gráfico 3
\[
\begin{gather}
{\large{\tau}}_{2}=nRT\ln\left(\frac{V_{2}}{V_{1}}\right)\\
{\large{\tau}}_{2}=600nR\ln\left(\frac{6,0}{3,0}\right) \tag{II}
\end{gather}
\]
representado pela área em cinza sob a isoterma de T2=600 K (em vermelho no gráfico).

A relação entre os trabalhos nas duas transformações é dada dividindo-se a expressão (I) pela expressão (II)
\[
\begin{gather}
\frac{{\large{\tau}}_{2}}{{\large{\tau} }_{1}}=\frac{600\cancel{n}\cancel{R}\cancel{\ln\left(\dfrac{6,0}{3,0}\right)}}{300\cancel{n}\cancel{R}\cancel{\ln\left(\dfrac{6,0}{3,0}\right)}}\\
\frac{{\large{\tau}}_{2}}{{\large{\tau}}_{1}}=\frac{600}{300}
\end{gather}
\]
\[ \bbox[#FFCCCC,10px]
{\frac{{\large{\tau} }_{2}}{{\large{\tau} }_{1}}=2}
\]
publicidade

Fisicaexe - Exercícios Resolvidos de Física de Elcio Brandani Mondadori está licenciado com uma Licença Creative Commons - Atribuição-NãoComercial-Compartilha Igual 4.0 Internacional .